مقدمه:
سرطان به نوعی از بیماریها گفته میشود که در آن گروهی از سلولها رشد غیر قابل کنترل پیدا نموده، به بافتهای مجاور حمله کرده و گاهی نیز از طریق خون یا لنف به نواحی دیگر بدن منتقل میگردند. در ایالات متحده از هر چهار مرگ یکی بهواسطه سرطان رخ میدهد (۱). تحقیقات در ایران نشان داده که سرطان پس از بیماریهای قلبی و تصادف، سومین علت منجر به مرگ است (۲).
سرطان ریه یکی از انواع رایج بدخیمی است که هردو جنس مذکر و مؤنث را درگیر کرده و بهعنوان دلیل اصلی مرگ ناشی از سرطان در سرتاسر دنیا شناخته میشود (۳). این سرطان اولین دلیل مرگ بهویژه در مردان، در سرتاسر دنیا است، با این حال در میان زنان، سرطان ریه چهارمین سرطان شایع و دومین دلیل مرگ بهحساب میآید. بر اساس آمار جهانی در سال ۲۰۱۳، سرطان ریه ۱۹/۵ درصد مرگ را به خود اختصاص داده است، بهطوریکه هرساله ۱/۳میلیون نفر در سرتاسر دنیا به دلیل ابتلا به سرطان ریه جان خود را از دست میدهند (۴ و ۵).
شیوع سرطان ریه در ایران با کشورهای دیگر متفاوت است، با این حال در سالهای اخیر شیب رو به افزایشی در شیوع سرطان ریه در ایران گزارش شده است. مطالعات آماری نشان میدهد الگوهای وقوع، مرگومیر و شیوع سرطان ریه در ایران یکسان و منطبق بر هم هستند و افزایش نرخ وقوع این سرطان در سالهای آتی پیشبینی شده است (۶).

انواع سرطان ریه
تاکنون گونههای مختلفی از سرطان ریه بر اساس مطالعات هیستولوژی و بررسی سلولهایی که دچار تراریختی و سرطان میشوند، شناسایی شده است که هریک نشانههای مربوط به خود را دارند.
· سرطان ریه با یاختههای کوچک {(SCLC) Small cell lung cancer}
یاختههای سرطانی گونه کوچک در زیر میکروسکوپ به مانند جوی دو سر دیده میشود و به آن سرطان جو مانند نیز گفته میشود. روند رشد اینگونه سرطان ریه تند است و در زمان کوتاهی در اندامهای دیگر پراکنده میشود. نزدیک ۲۰% سرطانهای ریه از اینگونه هستند (۷ و ۸).
- سرطان ریه نوع غیر یاخته کوچک {Non-small cell lung cancer (NSCLC)}
اینگونه سرطان ریه با در نگریستن به گونه سلول پدیدارشده در بافت ریه که دچار تراریختی و سرطان شده است دستهبندی میشود؛ از این رو گونههای زیادی از این سرطان شناخته شده است. این دسته خود مشتمل بر انواع آدنوکارسینوما (AC)، کارسینوم سلول سنگفرشی (SCC) و کارسینوم سلول بزرگ (LCC) است. در صورت شناسایی بهموقع این نوع سرطان ریه میتوان به بهبودی بیمار امید داشت (۹ و ۱۰).

فاکتورهای خطر برای سرطان ریه
فاکتورهای خطر شناساییشده برای سرطان ریه شامل مصرف دخانیات، آلایندههای پایدار، فاکتورهای ایمونوژنتیک و سن هستند. به غیر از مصرف دخانیات که عامل بیش از ۹۰ درصد موارد سرطان ریه است، تغییرات اپیژنتیکی و ژنتیکی مختلفی نیز که باعث فعال شدن انکوژنها و غیرفعال شدن ژنهای سرکوبگر تومور میشوند از علل بروز سرطان ریه میباشند (۱۱ و ۱۲).
تشخیص سرطان ریه
با نگریستن در میزان تندرستی بیمار، روند شناسایی سرطان ریه دربرگیرنده این آزمونها است:
عکسبرداری از ریهها با تابش پرتو X، آزمایش خلط، سیتیاسکن، سیتیاسکن گردان یا اسپایرال، پرتونگاری با بهرهگیری از میدان مغناطیسی افزاینده و بیوپسی (۱۳-۱۹).
ژنها و مسیرهای سیگنالی دخیل در سرطان ریه نوع غیر یاخته کوچک
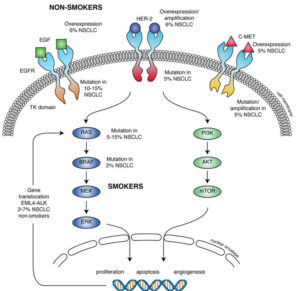
همانطور که گفته شد سرطان ریه نوع غیر یاخته کوچک (NSCLC) حدود ۸۵ درصد از موارد سرطان ریه را به خود اختصاص میدهد. مطالعات اخیر بر روی اساس مولکولی و مسیرهای سیگنالی دخیل در سرطان ریه منجر به شناسایی انواع مسیرهای سیگنالی و ژنهایی شده است که تنظیم آنها در روند تومورزایی در سرطان ریه دچار اختلال میشود. مطالعات بالینی نشان داد که حدود ۹۸ درصد از ردههای سلولی سرطان ریه دارای تغییرات ژنتیکی در حداقل یکی از ژنهای TP۵۳ (۷۹%)، CDKN۲A (۵۹%)، RB۱ (۳۵%)، STK۱۱ (۲۷%)، خانوادهی MYC (۲۰%)، KRAS (۱۷%)، PTEN (۱۱%)، PIK۳CA (۸%)، EGFR (۷%)، NRAS (۶%)، MET (۵%)، BRAF (۲%)، HER۲ (۲%) و یا AKT و EML۴-ALK هستند. جالب است که جهشهای ژنی EGFR، HER۲، BRAF، KRAS و NRAS، جزء جهشهای غالب در آدنوکارسینومای ریه هستند، درحالیکه جهش PIK۳CA در هم سرطان ریهی غیر یاخته کوچک و هم در نوع یاخته کوچک مشاهده میشود؛ بهعلاوه مشخص شده است احتمال بروز جهشهای همزمان در ژنهای مربوط به یک مسیر سیگنالی کمتر از بروز تنها یک جهش ژنی است، بهطوریکه در ۲۸ درصد ردههای سلولی سرطان ریه تنها یک موتاسیون در یک ژن شناسایی شد، درحالیکه ۲۶ درصد دو یا سه موتاسیون همزمان را نشان دادند (۲۰)
.
درمان
به علت میزان مرگومیر بالای ناشی از سرطان ریه و فراوانی این سرطان در هر دو جنس، نیاز به توسعه روشهای جدید و مؤثر درمانی بسیار احساس میشود. درمانهای معمول برای سرطان ریه در مراحل اولیه شامل جراحی و برداشت توده توموری، استفاده از شیمیدرمانی و در نهایت رادیوتراپی است. تمام این روشها دارای عوارض جانبی مخصوص به خود هستند که بسیاری از آنها هنوز بهطور دقیق شناسایی نشده است. اخیراً هدفدرمانی مولکولی (Molecular Target Therapy) با هدف درمان اختصاصی برای هر نوع سرطان بر پایه پزشکی شخصــــــــــی (Personalized Medicine) و البته کمترین عارضه جانبی بسیار مورد توجه قرار گرفته است.
اکثر روشهای درمانی مولکولی سرطان ریه بر روی گیرندههای تیروزین کینازی که مسئول رشد و بقای سلول میباشند، تمرکز کرده است. گیرندههای تیروزین کینازی معمولاً در سرطان ریه NSCLC دچار موتاسیون میشوند. این موتاسیونها اغلب منجر به افزایش فعالیت این گیرندهها و در نتیجه فعال شدن مسیرهای سیگنالینگ پاییندستی و سلسله اتفاقاتی میشود که در مجموع سبب گسترش تومور (Tumor Progression) میگردد (۲۱). گیرندههای تیروزین کینازی متنوعی در سطح سلول وجود دارد که مهمترین آنها گیرنده فاکتور رشد اپیدرمال (EGFR)، گیرنده فاکتور رشد هپاتوسیت HGFR/c-MET و آناپلاستیک لنفوما کیناز (ALK) هستند. این گیرندهها اغلب در درمانهای مولکولی مورد هدف قرار میگیرند. یکی دیگر از مولکولهایی که در هدف درمانی مورد توجه قرار میگیرد (BRAF) است (۲۲). موتاسیون در دومین تیروزین کینازی این گیرندهها باعث upregulation و افزایش فعالیت مسیرهای سیگنالینگ پاییندستی نظیر MAP-kinase، PI۳K/Akt و mTOR خواهد شد (۲۳). این مسیرهای سیگنالینگ مسئول بقا (Survival)، تکثیر (Prolifration)، مهاجرت (Migration) و رگزایی (Angiogenesis) در سلولهای سرطانی هستند (۲۴). داروهای مهارکننده تیروزین کیناز از طریق اتصال به دومین تیروزین کینازی گیرندههای فوق و مهار فعالیت آنها سبب کاهش فعالیت مسیرهای سیگنالینگ پاییندستی شده و از پیشرفت سرطان پیشگیری میکنند (۲۵). مطالعات نشان داده است که علت بروز ۸۰ درصد از موارد NSCLC، بروز تغییرات ژنتیکی در گیرندههای تیروزین کینازی و فعالیت بیش از حد آنها و افزایش فعالیت دو مسیر سیگنالینگ مهم پاییندستی یعنی RAS/RAF/MAPK و PI۳K/Akt/mTOR است (۲۶). داروهایGefitinib و Erlotenib- داروهای نسل اول و دوم هدف درمانی در -NSCLC که با اتصال به دومین تیروزین کینازی ملکول EGFR باعث مهار مسیرهای سیگنالینگ پاییندستی میشوند از اقبال بالایی برخوردار هستند.
شیمیدرمانی
به استفاده از داروهای آنتینئوبلاست به منظور کشتن سلولهای تومور از طریق مداخله کردن در کارکردهای سلولی و تولید مثل آنها شیمیدرمانی گفته میشود (۳۲). داروهای شیمیدرمانی بیشترین تأثیر را بر روی سلولهای دارای بیشترین سرعت تکثیر دارند (۳۲). هدف شیمیدرمانی کنترل و تسکین بیماری است (۲۷).
شیمیدرمانی ترکیبی مبتنی بر پلاتین؛ یک روش درمانی استاندارد برای درمان کمکی در NSCLC به دنبال عمل جراحی است. سیسپلاتین (Cisplatin) رایجترین داروی شیمیدرمانی است که از تکثیر DNA جلوگیری میکند و ساختار غشای سلولی را از بین میبرد. سیسپلاتین با آسیب رساندن به DNA و ایجاد مرگ سلولهای توموری نقش مهمی در درمان NSCLC دارد. تعداد فزایندهای از مطالعات ثابت کردهاند که حساسیت به شیمیدرمانی از فردی به فرد دیگر متفاوت است، زیرا تغییرات زیادی بین افراد مختلف در ظرفیت پاسخ به آسیب DNA و ترمیم آن وجود دارد. مطالعات قبلی نشان دادهاند که سلولهای NSCLC با وضعیت عملکردی متفاوت پاسخهای متفاوتی به سیسپلاتین نشان میدهند (۲۸).
آنچه در درمان سرطان ریه مشکلآفرین است، بروز مقاومت دارویی نسبت به داروهای هدف درمان و شیمیدرمانی است. علل بروز مقاومت دارویی در این بیماری بسیار پیچیده است و عوامل مختلفی در آن دخیل هستند. مطالعات اخیر نقش microRNAها و long non-codingRNA را در بروز مقاومت بسیار پررنگ نشان داده است (۲۹ و ۳۰). محققان همچنان در صدد یافتن راههای مقابله با بروز مقاومت دارویی و افزایش مدت بقا در بیماران هستند.
فراپژوهش