مطالعات اخیر نشان دادهاند که درمان توکسوپلاسموز در حین بارداری به کاهش انتقال بیماری به جنین و عواقب بالینی آن کمک میکند. هرچه درمان سریعتر باشد عواقب بهتری خواهد داشت، لذا روشهای آزمایشگاهی باید به تشخیص بههنگام توکسوپلاسموز مادرزادی کمک نمایند.
شناسایی آنتیبادیهای توکسوپلاسما از جنس IgG، IgM و IgA و اخذ شرححال کامل مادر بهویژه سن جنین در هنگام آلودگی به توکسوپلاسما، حداقلهای لازم برای تشخیص میباشند. در این مقاله به مرور روشهای آزمایشگاهی برای تشخیص توکسوپلاسموز مادرزادی و بهویژه روشهای سرولوژیک خواهیم پرداخت، همچنین یک الگوریتم تشخیصی که در آن شرححال مادر هم لحاظ شده است، عرضه میشود.
در سال ۱۹۳۹ ولف و همکارانش (۱) برای اولین بار گزارش نمودند که انگل توکسوپلاسما گوندی برای انسان پاتوژن تلقی شده و میتواند بیماری مادرزادی ایجاد نماید (۲،۱). بلافاصله بعد از این اکتشاف مشخص شد که طیف بالینی توکسوپلاسموز مادرزادی میتواند از فرد ظاهراً سالم تا اختلالات شدید نورولوژیک و بینایی و حتی مرگ متغیر باشد (۳). اکنون کاملاً مشخص است که توکسوپلاسموز مادرزادی گستره جهانی دارد و میزان وقوع آن۱۹۰/۰۰۰ مورد در سال میباشد (۴). با این وصف مرگومیر ناشی از این بیماری قابل پیشگیری و درمان میباشد (۳).
درمان بههنگام بیماری یعنی زمانی که هنوز جنین متولد نشده است میتواند از انتقال بیماری به جنین جلوگیری کرده و عواقب بالینی آن را بهبود بخشد (۱۰-۵)، لذا ضرورت دارد که تستهای آزمایشگاهی برای تشخیص توکسوپلاسموز مادرزادی حساس و اختصاصی بوده و قدرت پیشبینی بالایی داشته باشند تا بتوان سریعاً جنین یا نوزاد مبتلا را شناسایی کرده و نسبت به درمان وی اقدام نمود. در این مقاله تستهای سرولوژیک که در حال حاضر برای تشخیص توکسوپلاسموز مادرزادی کاربرد دارند را مورد بررسی قرار میدهیم. روشهای دیگر همچون PCR، رنگآمیزیهای بافتی، جداسازی انگل از موش، تصویربرداری از مغز و سایر ناهنجاریهای آزمایشگاهی نیز مورد اشاره واقع خواهند شد، اما بررسی جزئیات آنها خارج از اهداف این مقاله میباشد، علاوه بر این شرححال مادر (همچون سن جنین در زمان آلوده شدن مادر و اینکه آیا مادر تحت درمان قرار گرفته یا نه ) نیز در الگوریتم تشخیصی لحاظ خواهد شد.
ملاحظات عمومی
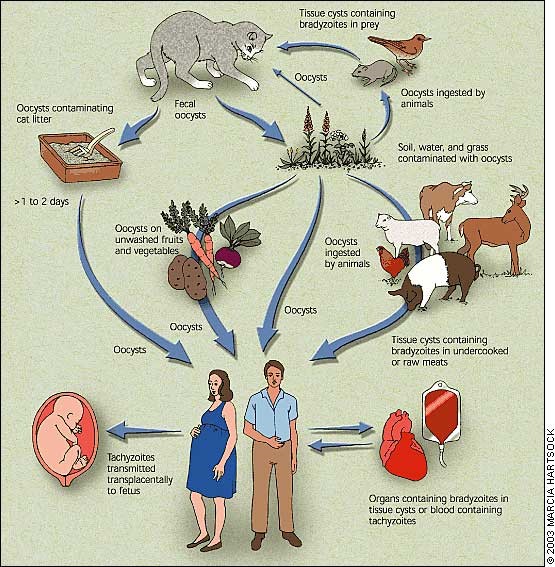
اگر مادر عفونت توکسوپلاسما را در طی حاملگی یا در موارد نادری اندک زمانی قبل از حاملگی کسب کند، احتمال وقوع توکسوپلاسموز مادرزادی وجود دارد.
عامل عفونت از سد جفتی– خونی عبور کرده و جنین را آلوده میسازد. سن جنین و درمان مادر دو عاملی هستند که میزان خطر انتقال را تعیین میکنند (۱۰-۵).
در مجموع خطر انتقال در مادرانی که در حین حاملگی تحت درمان قرار گرفتهاند حدود ۳۰% است، گرچه میزان انتقال، به سن جنین در هنگام آلوده شدن مادر بستگی تام دارد و از ۱۵% در هفته سیزدهم به ۴۴% در هفته ۲۶ و ۷۱% در هفته ۳۶ میرسد. البته این مربوط به مادرانی است که درمان میشوند (۱۱،۱۰). ممکن است در مادرانی که در گذشته دور مبتلا به توکسوپلاسما بودهاند بر اثر تضعیف سیستم ایمنی، عفونت نهفته فعال شده و موجب توکسوپلاسموز مادرزادی گردد که البته این اتفاق خیلی معمول نیست.
تشخیص یا رد تشخیص توکسوپلاسموز مادرزادی نیازمند اطلاعات و شرححال دقیق و جامع از مادر و فرزند میباشد. این اطلاعات بر تفسیر نتایج آزمایشگاهی شدیداً تأثیرگذار خواهند بود (۱۳،۱۲).
مطلوب است که وضعیت مادر به لحاظ داشتن نقص ایمنی یا سلامت ایمنی معلوم شده و مشخص گردد که در کدامیک از گروههای زیر قرار میگیرد:
- قبلاً به عفونت توکسوپلاسما مبتلا نشده و تا یک ماه پس از تولد نوزاد هم آزمایش خون وی منفی است (خطر توکسوپلاسموز مادرزادی وجود ندارد).
- عفونت مزمن، مادر قبل از حاملگی به توکسوپلاسما آلوده شده است (خطر توکسوپلاسموز مادرزادی وجود ندارد مگر آنکه سیستم ایمنی مادر اختلال داشته باشد).
- عفونت حاد، مادر در طی دوران حاملگی یا سه ماه قبل از آن دچار عفونت شده است (خطر ابتلا به توکسوپلاسموز مادرزادی وجود دارد).
در مورد گروه سوم زمان عفونت در طی حاملگی، درمان با داروهای ضد توکسوپلاسما و نوع دارو اهمیت دارد، چرا که تفسیر نتایج آزمایشگاهی به این عوامل بستگی دارد (۱۴). بهعنوان نمونه در مادرانی که در ابتدای حاملگی به عفونت مبتلا شدهاند و یا در هنگام حاملگی داروی ضد توکسوپلاسما دریافت کردهاند در مقایسه با آنهایی که در اواخر حاملگی مبتلا شده و یا دارو دریافت نکردهاند، حساسیت آزمایش سرولوژیک در نوزادان گروه اول کمتر میباشد (۱۴).
اطلاعات مربوط به وجود علائم بالینی در جنین.و نوزاد به تفسیر آزمایش و نیز فواصل زمان پایش پس از تولد و نیز تشخیص ضرورت انجام آزمایشهای دیگر (همچون PCR) کمک میکند.
اصول و روشهای موجود برای تشخیص توکسوپلاسموز مادرزادی
روشهایی همچون بررسی پاسخ ایمنی هومورال به توکسوپلاسما، تکثیر DNAی انگل، تشخیص آنتیژن اختصاصی توکسوپلاسما در بافت و جدا کردن انگل در طی دهههای اخیر مورد استفاده بودهاند (جدول ۱) (۱۷-۱۵).
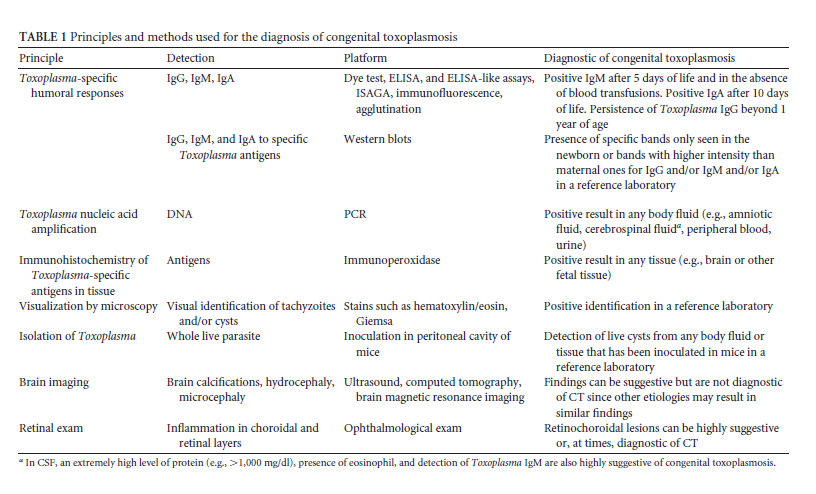
تشخیص توکسوپلاسموز مادرزادی در جنین
در زمان حاملگی حضور انگل در مایع آمنیوتیک (تکثیر DNA، میکروسکوپی یا جدا کردن ارگانیسم) و یا در بافت جنین (تکثیر DNA، رنگآمیزی آنتیژن، میکروسکوپی یا جدا کردن ارگانیسم) تشخیص توکسوپلاسموز مادرزادی را محرز میکند (جدول ۱). معمولترین و مقبولترین روش تشخیص توکسوپلاسموز مادرزادی در دوران حاملگی استفاده از PCR در مایع آمنیوتیک میباشد.
تشخیص توکسوپلاسموز مادرزادی در نوزادان و اطفال
روش طلایی برای تشخیص توکسوپلاسموز مادرزادی پس از تولد باقی ماندن حضور IgG اختصاصی توکسوپلاسما تا ۱۲ ماهگی است. رد تشخیص توکسوپلاسموز مادرزادی هم با کاهش تیتر این آنتیبادی تا حد ناپدید شدن بدون اقدام درمانی قبل از دوازده ماهگی میباشد. (شکل ۱).
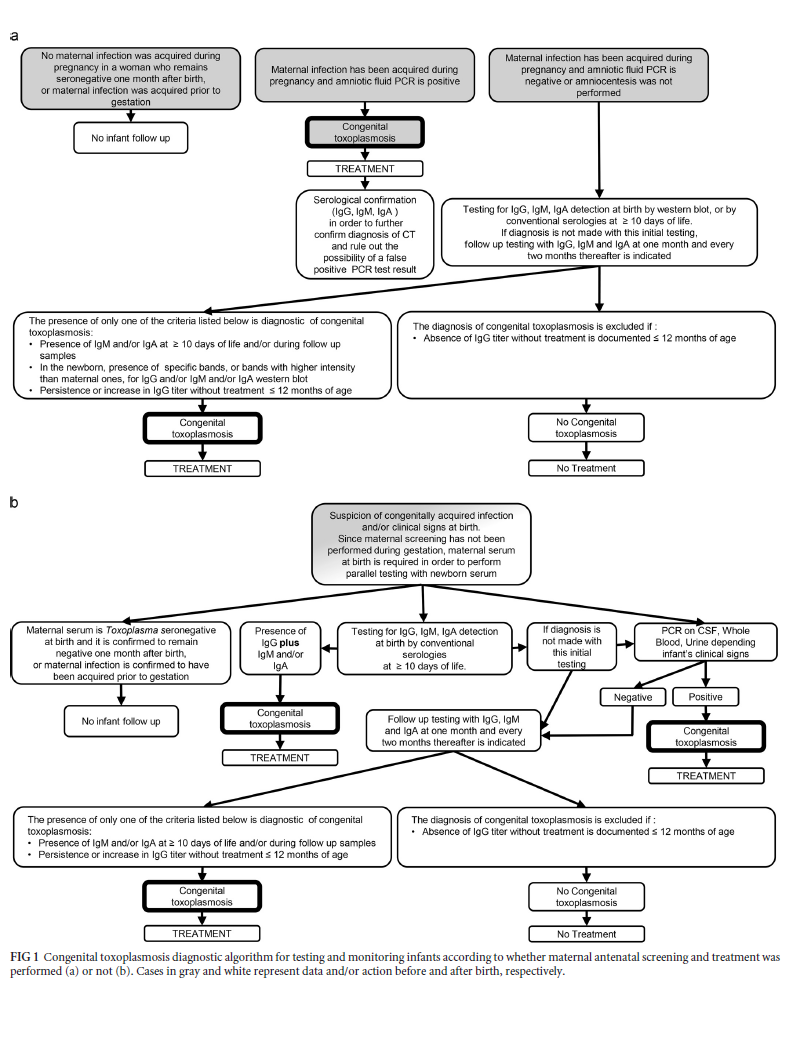
در غیاب اطلاعات و شرححال و سوابق بالینی، تشخیص توکسوپلاسموز مادرزادی بعد از سال اول تولد مشکل میشود چرا که این احتمال هست که نوزاد عفونت را پس از تولد گرفته باشد، لذا معقول است که تمام تلاشهای لازم جهت تعیین تکلیف ابتلا به توکسوپلاسموز مادرزادی در هنگام حاملگی یا سال اول تولد به عمل آید.
معمولترین روش آزمایشگاهی برای تشخیص توکسوپلاسموز مادرزادی در نوزادان استفاده از روش سرولوژی در تشخیص ایزوتایپهای مختلف آنتیبادی توکسوپلاسما در سرم میباشد. صرفنظر از روش شناسایی آنتیبادی توکسوپلاسما، لازم است که IgG، IgM و IgA هر سه با هم انجام شوند چراکه حساسیت مجموع آنها بیشتر میباشد (۱۳،۱۸-۱۵).
PCR توکسوپلاسما در مایع نخاع و خون محیطی و ادرار روش دیگری است که میتوان در تشخیص زودهنگام توکسوپلاسموز مادرزادی از آن استفاده کرد. این روش بهویژه در مناطقی که برنامههای غربالگری و درمان قبل از تولد وجود ندارد، مفید خواهد بود (۱۹).
برای شناسایی IgG توکسوپلاسما، روش رنگ روش مرجع و استاندارد طلایی میباشد، اما این روش به جهت نیاز به حضور انگل زنده، تنها در مراکز رفرانس قابل انجام است. الیزا و روشهای مشابه الیزا، آگلوتیناسون و ایمونوفلورسانس غیرمستقیم روشهای دیگری هستند که در تشخیص توکسوپلاسما استفاده میشوند.
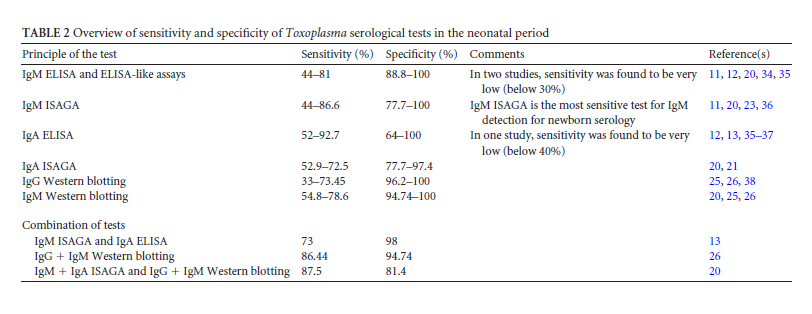
در خصوص شناسایی IgM توکسوپلاسما، علاوه بر روشهای دیگر که در مورد IgG استفاده میشود (ISAGA) Immuno Sorbent Agglutination Assayهم به کار میرود که حساسیت آن نسبت به روش الیزا بالاتر است (۸۱/۱% در مقایسه با ۶۴/۸%) (۲۰). برای نوزادان کمتر از شش ماه روش ISAGA IgM روش انتخابی محسوب میگردد (۲۰).
برای تشخیص Toxoplasma IgA روشهای الیزا در دسترس میباشد، اما در برخی آزمایشگاهها در این مورد هم روش ISAGA ترجیح داده میشود (۲۱،۲۰).
گرچه در برخی مطالعات اولیه سنجش IgE Toxoplasma امیدوارکننده بود، اما بعدها مشخص گردید که هیچ مزیتی نسبت به مجموع IgM و IgA ندارد (۲۳،۲۲).
بعد از تولد این اشکال وجود دارد که چگونه IgG نوزاد را از IgG منتقل شده از طریق جفت متمایز نماییم. از طرفی در پنج روز اول تولد IgM و در ۱۰ روز اول تولد IgA مادر هم ممکن است در سرم نوزاد وجود داشته و ایجاد تداخل نماید. برای غلبه بر این مشکل روشهایی همچون وسترنبلات برای تفکیک آنتیبادی مادر از نوزاد بکار گرفته میشوند.
در وسترنبلات باندهای مختلفی ظاهر میشود که نشانه اتصال بین IgG، IgM و IgA بیمار با آنتیژنهای مختلف توکسوپلاسما میباشند. بهمنظور افتراق بین توکسوپلاسموز مادرزادی و ساخت آنتیبادی توسط خود نوزاد، باندهای ایجاد شده از سرم مادر و نوزاد مقایسه میگردند. وجود باندهایی در سرم نوزاد که در نمونه مادر نیست و یا ضخیمتر بودن باند نوزاد به این افتراق کمک میکند. روش وسترنبلات در مقایسه با روشهای سرولوژیک متداول سه ماه زودتر تشخیص را ممکن میسازد (۲۴). تلفیق روش وسترنبلات و سرولوژی حساسیت بالاتری نسبت به تکتک این روشها دارد، اما باید توجه داشت که بعد از سن خاصی موارد مثبت کاذب وسترن بلات افزایش مییابد و لذا تفسیر آن مشکل میگردد (در بعضی از کیتها برای IgG و IgM توکسوپلاسما بعد از ۱ و ۳ ماهگی مثبت کاذب دیده میشود) (۲۶،۲۵،۱۷).
آزمایشگاههای بسیاری هستند که میتوانند برای توکسوپلاسما IgG، IgMو PCR انجام دهند اما تستهایی همچون ISAGA IgM، وسترنبلات و جداسازی انگل فقط در آزمایشگاههای رفرانس انجامپذیر هستند و در نوزادان صحهگذاری شدهاند. ترکیب اینها با آزمایشهای متداول حساسیت را افزایش میدهد (۲۳،۲۰).
روشهای محدود دیگری هم برای تشخیص توکسوپلاسموز مادرزادی توصیف شدهاند.
روش (ELIFA) Enzyme – Linked Immune Filtration Assay راه دیگری برای مقایسه پروفایل ایمونوگلوبینهای مادر و نوزاد است که تنها در چند آزمایشگاه محدود قابل انجام میباشد (۲۰).
با تحریک آنتیژنهای توکسوپلاسما از سلولهای T، اینترفرون گاما آزاد میشود که سنجش آن در تشخیص توکسوپلاسموز مادرزادی مفید است، اما هنوز بهطور تجاری در دسترس نیست (۲۷).
سنجش IgG Toxoplasma در بزاق نوزاد نیز روش امیدوارکنندهای برای تشخیص توکسوپلاسموز مادرزادی است (۲۸). علاوه بر این تصویربرداری از مغز و معاینه چشم هم میتواند اطلاعات مفیدی برای تشخیص توکسوپلاسموز مادرزادی ارائه کنند (جدول ۱).
رویکرد کلی تشخیصی
توکسوپلاسموز مادرزادی را میتوان در دوران جنینی یا زمان پس از تولد تشخیص داد. برحسب اینکه مادر قبلاً مورد آزمایش و درمان قرار گرفته باشد و اینکه برای تشخیص جنین از آمنیوسنتر استفاده شده باشد یا نه، رویکرد تشخیص در نوزادان فرق میکند. غربالگری و درمان روتین قبل از تولد تنها در چند کشور انجام میشود (اتریش، بلژیک فرانسه، نروژ، اروگوئه و برخی مناطق در ایتالیا و برزیل)، لذا پزشکان این مناطق اطلاعاتی همچون نتایج سرولوژی مادر، نتایج PCR مایع آمنیوتیک، سن دقیق جنین به هنگام ابتلای مادر و سابقه درمان ضد توکسوپلاسما را در اختیار خواهند داشت.
اما بیشتر نوزادان دنیا در مناطقی متولد میشوند که چنین برنامههایی اجرا نمیشود (۲۳). فقدان یا نقص غربالگری پیش از تولد توکسوپلاسما و درمان آن یکی از فاکتورهای مهم خطر برای توکسوپلاسموز مادرزادی محسوب میگردد (۲۹).
تفاوت در رویکرد تشخیص توکسوپلاسموز مادرزادی بر اساس بود و نبود برنامههای غربالگری و درمان مادران
تفاوتهای مهمی در رویکرد، عملکرد و استفاده از روشهای آزمایشگاهی توکسوپلاسموز مادرزادی در مناطقی که غربالگری پیش از تولد انجام میشود با مناطق دیگر وجود دارد (شکل ۱). هدف اصلی برنامههای غربالگری توکسوپلاسما در مادران، تشخیص هرچه سریعتر عفونت حاد در حاملگی میباشد. مادران در معرض خطر (افراد seronegative) در اولین ویزیت پیش از تولد مشخص شده و در فواصل زمانی معین مورد ارزیابی و پایش قرار میگیرند (۳).
این رویکرد امکان درمان سریع در مادرانی که در حین حاملگی آلوده میشوند را فراهم میکند. این استراتژی انتقال عفونت به جنین و عوارض شدید و مرگ را در وی کاهش میدهد (۹)، لذا در مناطقی که غربالگری انجام میشود تشخیص و درمان عفونت در جنین و نوزاد زودتر اتفاق میافتد. پیامد ناخواسته غربالگری و درمان در این مناطق کاهش حساسیت روشهای آزمایشگاهی همچون سرولوژی و PCR در این مناطق است (۲۳،۱۲)، اما پزشکان این مناطق دسترسی سریع به اطلاعات و سرم مادر دارند که این امر نقش مهمی در انتخاب روش تشخیص آزمایشگاهی توکسوپلاسموز مادرزادی دارد؛ بهعنوان مثال اطلاع دقیق از سن جنین به هنگام ابتلای مادر، انجام درمان ضد توکسوپلاسما برای مادر و داروی انتخابی از جمله اطلاعاتی هستند که به انتخاب روش آزمایشگاهی تشخیص توکسوپلاسموز مادرزادی کمک میکنند.
در مناطقی که برنامه غربالگری اجرا نمیشود این اطلاعات حیاتی در خصوص مادر معمولاً در دسترس نمیباشد. این نقص اطلاعات موجب میشود در نوزادی که نیاز به آزمایش ندارد آزمایش انجام شود و در نوزادی که نیاز به درمان دارد اقدام درمانی با تأخیر صورت پذیرد (۲۳).
در مناطق بدون غربالگری فقدان اطلاعات در خصوص مادر سبب میشود که استفاده از PCR برای تشخیص عفونت نوزادان افزایش یابد چراکه تصور میشود حساسیت این روش بالاتر باشد (۲۳،۱۹).
مشابهت رویکرد تشخیصی توکسوپلاسموز مادرزادی در حضور یا غیاب برنامه غربالگری و درمان مادر
در مواردی که نوزاد در یکی از گروههای ذیل واقع شود رویکرد سرولوژیک تشخیص توکسوپلاسموز مادرزادی در مناطقی که غربالگری انجام میشود با مناطق دیگر یکسان است (شکل ۱):
- چون مادر و نوزاد هردو از نظر سرولوژیک منفی هستند، لذا احتمال توکسوپلاسموز مادرزادی وجود ندارد.
- بهواسطه ابتلای مزمن مادر احتمال توکسوپلاسموز مادرزادی وجود ندارد (مگر درصورتیکه شدیداً از نظر ایمنی مشکل داشته باشد).
- احتمال توکسوپلاسموز مادرزادی وجود دارد چون که مادر در حین حاملگی مبتلا شده (یا مشکوک به ابتلا میباشد) و یا نوزاد علائم بالینی عفونت را در بدو تولد نشان میدهد. مادرانی که آزمایش سرمی آنها در هنگام حاملگی و یک ماه بعد از زایمان منفی بوده در معرض توکسوپلاسموز مادرزادی نمیباشند، لذا پایش سرولوژیک نوزادان آنها ضرورت ندارد. علت اینکه یک ماه بعد از تولد باید آزمایش سرولوژیک از مادر بعمل آید این است که احتمال اندکی وجود دارد که کمی قبل از زایمان عفونت حادث شده باشد.
در خصوص مادرانی که قبل از حاملگی دچار عفونت شدهاند احتمال توکسوپلاسموز مادرزادی منتفی است مگر اینکه در طی حاملگی شدیداً دچار مشکل ایمنی همچون ایدز گردند. در خون نوزادان این مادرها IgG وجود دارد که از جفت منتقل شده و نیاز به پایش سرولوژیک نیست. اما در مناطقی که غربالگری توکسوپلاسما وجود ندارد اطمینان از اینکه ابتلای مادر به توکسوپلاسما قبل از حاملگی بوده است غالباً غیرممکن است. اغلب موارد اولین آزمایش سرمی در سهماهه سوم یا حتی به هنگام تولد انجام میشود. در چنین مواقعی اگر نتایج سرولوژیک از نظر IgG و IgM مثبت باشد تنها در آزمایشگاههای مرجع به کمک آزمایشاتی چون تست رنگ IgG، الیزا برای IgM، آویدیتی، آگلوتیناسیون افتراقی (فیکس تاکیزوئیت با استون در برابر فرمالین) و الیزای IgA و IgE میتوان برای فهم ابتلای مادر به عفونت قبل از بارداری تلاش کرد (۳۱،۳۰).
مادرانی که در هنگام حاملگی یا اندکی قبل از آن به توکسوپلاسما مبتلا شوند در معرض توکسوپلاسموز مادرزادی میباشند. اگر درمان با اسپیرامایسین شروع شود خطر کاهش مییابد. در آمریکا این دارو به رایگان در دسترس است. در مناطقی که برنامه غربالگری اجرا میشود اگر در حین حاملگی واکنش سرمی مادر مثبت شود ابتلای تازه به عفونت محرز میگردد. در سایر مناطق که این آزمایش انجام نمیشود معمولاً تشخیص تا هنگام بروز علائم در جنین یا نوزاد به تأخیر میافتد. در مواردی که تنها امکان آزمایش دیرهنگام بر سرم مادر وجود دارد احتمال تعیین عفونت مزمن و قبلی مادر تنها در آزمایشگاههای مرجع امکانپذیر است.
آزمایشهای سرولوژیک در نوزادان این مادران هم به تأئید یا رد تشخیص توکسوپلاسموز مادرزادی کمک میکنند. در نوزادانی که قبلاً آزمایش PCR مایع آمنیوتیک در آنها مثبت شده برای تأئید تشخیص توکسوپلاسموز مادرزادی و کسب اطلاعات بیشتر در مواردی که احتمال مثبت کاذب در PCR وجود دارد، باز هم انجام آزمایش سرولوژی توصیه میگردد. در نوزادانی که تست PCR آمنیوتیک منفی بوده یا انجام نشده است، پایش با آزمایشات سرولوژی کاربرد تشخیصی دارد. صرفنظر از انجام آزمایش PCR و نتیجه آن پانل سرولوژی شامل آنتیبادیهای IgG، ISAGA IgM و IgAی توکسوپلاسما در نوزاد باید انجام پذیرد. اولین نمونهگیری باید ۱۰ روز پس از تولد باشد تا از تداخل آنتیبادی مادر اجتناب شود.
برای پیگیری باید در فواصل ۱ ماه، ۲ ماه، و هر دو ماه یک بار نمونهگیری بعمل آید (شکل ۱). نوزاد هر مادری که در طی حاملگی یا اندکی قبل از آن آلوده شده باشد باید تا یک سالگی با روش سرولوژی مورد پایش قرار گیرد. در نوزادانی که مبتلا نیستند مقدار IgG علیه توکسوپلاسما هر ماه تقریباً نصف میشود و در حوالی ۶ یا هفتماهگی از بین میرود اما در نوزاد مبتلا تا ۱۲ ماهگی از بین نمیرود. در برخی از نوزادان که ابتلای مادرزادی دارند مصرف داروی Pyrimethamine به همراه سولفامید باعث منفی شدن IgG علیه توکسوپلاسما میگردد و این تصور را به وجود میآورد که نوزاد ابتلای مادرزادی نداشته است ولی قطع درمان در این نوزادان سبب بازگشت مجدد تیتر مثبت IgG میشود. اگر با قطع درمان، IgG همچنان منفی باقی بماند تشخیص توکسوپلاسموز مادرزادی رد میشود.
مسیر آینده
تشخیص آزمایشگاهی توکسوپلاسموز مادرزادی از طرق و روشهای مختلفی بهره میبرد (شکل ۱). تحقیقات آینده باید هزینه و عملی بودن شناسایی آنتیبادیها، DNA و انگل زنده را در سطوح مختلف مشخص نماید؛ بهعنوان مثال تشخیص همزمان چند آنالیت بر روی یک نمونه گزینه جالبی خواهد بود که IgG، IgM و IgA توکسوپلاسمایی را به همراه سایر پاتوژنهایی که ممکن است عفونت مادرزادی ایجاد نمایند، بهطور همزمان اندازه بگیرد (۳۳،۳۲). استفاده از پلتفرمی که ظرفیتهای متعدد دارد هزینه را کاهش داده و مزیت دیگر آن بررسی همزمان عفونتهای دیگر میباشد، علاوه بر این امکان انجام آزمایش آنتیبادی در سایر اجزای بدن همچون خون کامل و بزاق، علاوه بر کاهش هزینه، رضایت بیشتر بیمار را نیز به همراه خواهد داشت (۲۸).
در پایان مقامات بهداشتی و سیاستهای ملی باید نسبت به تأسیس آزمایشگاههای مرجع برای تشخیص و مدیریت توکسوپلاسموز مادرزادی اقدام نمایند چرا که این عفونت معمولاً در مطب و مراکز خصوصی به چشم نمیآید، اما میتواند سرمنشأ مرگومیر قابلتوجه در جنین و نوزادان باشد.
فراپژوهش