آسم یک تشخیص مهم برای تامینکنندگان مراقبتهای اولیه محسوب میشود، چرا که تشخیص آن خارج از آزمایشگاه و مبتنی بر معاینه بالینی است. احتمالاً تاکنون محققان در مدرسه پزشکی مونت سینایی نیویورک در خصوص استفاده از تست RNA بر روی شستشوی بینی در حال تحقیق هستند.

Bunyavanich دستیار مدیر در مؤسسه آلرژی غذایی Jeffe و دانشیار در Mount Sinai، برای دستیابی به یک منبع الهام، لازم نبود راه خیلی دوری برود. او یک کلینیک ایمونولوژی و آلرژی اطفال را اداره مینماید که در آنجا هر هفته با واقعیتهای درمان آسم مواجه میشود. او چنین توضیح میدهد:«من بیمارانی را میبینم که با ابزارهای کنونی ما در کشاکش هستند. تلاش برای بهدست آوردن اطلاعات عینی، وابسته به آسپیرومتری بوده که خود میتواند مشکلساز باشد. در بسیاری از مراکز مراقبتهای اولیه، شما در همان لحظه آسپیرومتری را در اختیار ندارید».
خود آسپیرومتری چالشهای خاص خود را نیز دارد؛ این تست نیازمند کارکنان آموزشدیده است و به انجام دقیق توسط بیماران بستگی دارد تا بتوان به اندازهگیریهای مناسب دست یافت. Bunyavanich چنین نتیجه گرفته است که «بیشتر بیماران انجام دادن آسپیرومتری را کار مشکلی میدانند».
دکتر راج کاپور، متخصص ریه و متخصص مراقبتهای ویژه و پزشکی خواب (sleep medicine) از این دیدگاه حمایت میکند؛ وی با اشاره به اینکه حداقل ۳۰ درصد تشخیصهای آسم توسط پزشکان اشتباه است، میگوید:«ضربالمثل قدیمی هر خسخسی آسم نیست که به پزشکی به نام Chevalier Jackson منتسب است، هیچگاه به اندازه امروز، مصداق نداشته است».

دکتر کاپور میگوید: «تشخیص نابجای آسم آلرژیک یا غیرآلرژیک میتواند به هفتهها، ماهها یا حتی سالها درمان غیرضروری با داروهای آلبوترول و کنترلکننده بیانجامد».
این نوآوری چیست؟
زمانی که Bunyavanich دوره فلوشیپ خود را میگذراند، درباره ارتباط بین بیولوژی نواحی فوقانی و نواحی تحتانی مجاری هوایی فکر میکرد.
این فیلد با در نظر گرفتن شماری از وضعیتهایی که با آسم همپوشانی دارند، در ارائه تعریف مشخصی از آسم مشکل دارد و علت آن تکیه بر یافتههای بالینی است که میتواند در این زمینه متغیر باشد. اگرچه بر اساس دستورالعملهای مرسوم، آسم را بیماری انسداد مجاری هوایی تحتانی میدانند، با این حال شواهد بیشتری نشاندهنده نقش مجاری هوایی فوقانی بهویژه بینی هستند. حداقل در نیمی از بیماران مبتلایان به آسم التهاب و سوزش بینی یا رینیت دیده میشود.
دکتر کاپور میگوید: «تشخیص صحیح آسم نمیتواند صرفاً بر مبنای شناسایی علائم انجام شود، زیرا علائمی مانند خسخس، سرفه و تنگی نفس در هنگام فعالیت، همگی غیراختصاصی هستند، بهعلاوه نتایج تستهای عملکرد ریوی غالباً در آسم نرمال هستند، حتی در مواردی که این تستها غیرطبیعی هستند باز نمیتوانند بین آسم، بیماری انسداد ریوی مزمن و سندرم همپوشانی آسم- بیماری انسداد ریوی مزمن افتراق ایجاد کنند».
ظهور مارکر زیستی بینی جهت آسم، راهی ساده برای تشخیص آسم از طریق برس زدن سلولهای بینی است که جایگزینی برای برخی نوآوریهــای دیگر- برای مثال آنالیز نیتریک اکساید بازدمی یا آنالیز سلولی خلط- که در دستیابی به مقبولیت ناکام بودهاند، است. Bunyavanich میگوید: «ما به چیزی نیاز داشتیم که بهراحتی قابل دستیابی باشد، استفاده از برس بینی تنها چند ثانیه وقت میگیرد».

این تست چگونه کار میکند؟
بیمار مینشیند و پزشک یک برس سیتولوژی را وارد بینی بیمار نموده و نمونه را جمعآوری مینماید. RNA بهدستآمده توالییابی میشود و الگوریتمها مبتلا بودن یا نبودن بیمار به آسم را پیشبینی میکنند.
محققان برای گسترش مدل خود از ۶۶ بیمار مبتلا به آسم از خفیف تا شدید و ۱۲۴ فرد سالم بهعنوان گروه کنترل، نمونه گرفتند (شکل ۱). تمرکز آنها بر روی آسم غیرشدید بود، زیرا چالشهای تشخیصی بیشتری در این گروه دیده میشد. از بین این افراد، ۱۵۰ نفر بهطور تصادفی جهت استفاده در طبقهبندی آسم اختصاص داده شدند و ۴۰ نفر باقیمانده دیگر جهت آزمایش توالییابی RNA دستهبندی شدند. محققان با انجام آنالیز افتراقی بیان ژن، به ۲۸۷۲ ژن دست یافتند که در مبتلایان به آسم، نسبت به گروه کنترل کمتر یا بیشتر بیان میشدند.
محدودیت آنالیز افتراقی بیان ژن این است که شما در هر بار میتوانید تنها به دنبال یک ژن بگردید. Bunyavinch میگوید: «این بهخوبی نشان نمیدهد که چه اتفاقی افتاده است؛ ژنها با یکدیگر میانکنش دارند. اگر شما در مورد بیولوژی فکر میکنید باید در مورد بیان جمعی و بههمپیوسته ژنها فکر کنید». برای بررسی اینکه آیا یک مجموعه کوچکتر از ژنها، بهواسطه میانکنش پیچیده آنها، میتواند آسم را بهتر طبقهبندی کند یا خیر؟ او با تیم خود یک مسیر یادگیری ماشین (machine learning pipeline) را راهاندازی کرد. آنها ابتدا انتخاب ویژگی را انجام دادند تا نسبت سیگنال به بینی را افزایش دهند. برای پیدا کردن این ویژگیها، آنها بهطور تکراری ویژگیها را با تعداد مختلف، انتخاب میکردند تا به تعداد مشخصی از ژنها دست پیدا کنند که بتواند با بیشترین دقت، وضعیت آسم را در مجموعه مورد آزمایش پیشبینی نمایند. در مرحله بعدی، طبقهبندی الگوریتمها از جمله رگرسیون نمایی (لجستیک) را بهکار گرفتند تا مدلهای طبقهبندی با آستانههای معین را ایجاد کنند و از آنالیز آماری برای انتخاب مدلی با بهترین عملکرد و کمترین تعداد ویژگیها استفاده کردند. طبقهبندی نهایی از ۹۰ ژن پیشبینیکننده تشکیل شده بود و از احتمال خروجی (probability output) به میزان > ۰/۷۶ بهعنوان آستانه خود برای مشخص کردن افراد مبتلا به آسم استفاده میکرد.
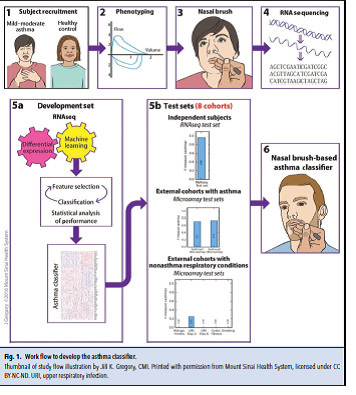
این مدل مختصر و مفید ۹۰ ژنی، در مقایسه با استفاده از بیان افتراقی تمامی ۲۸۷۲ ژن، عملکردی بهتر داشته است. Bunyavanich میگوید: «ژنها میتوانند در مسیرهایی که قابل شناسایی نیستند، شرکت کنند. روشهای سنتی و مرسوم از جمله بیان افتراقی به دلیل آنکه نمیتوانند چندین لایه اطلاعاتی را درهم ادغام کنند، روشهای محدودی هستند».
این پژوهشگران برای معتبر ساختن طبقهبندی خود، آن را بهصورت ۸ مجموعه آزمایشی اجرا کردند و نتایج مؤثر و گیرایی بهدست آمد. در بین مجموعه RNAseq متعلق به ۴۰ نفر، این روش طبقهبندی مقدار پیشبینی مثبت (positive predictive value) برابر ۱٫۰ و مقدار پیشبینی منفی معادل ۰/۹۶ با ناحیه زیر نمودار معادل ۰/۹۹۴ را نشان داد. این روش هنگامی که بر روی ۵ گروه مبتلا به رینیت آلرژیک، عفونت تنفسی فوقانی، فیبروزیس کیستیک و افراد سیگاری اجرا شد، نتیجه مثبت کاذب در حد صفر بود. این تست بر روی دو مجموعه از نمونههای asthma-control microarray نتوانست به همین اندازه خوب عمل کند و مقدار پیشبینی مثبت ۰/۹۳ یا ۰/۶۱و مقدار پیشبینی منفی ۰/۳۱یا ۰/۶۷ را نشان داد. پژوهشگران این امر را به «تفاوتها، در طراحی مطالعه و فاکتورهای تکنیکی بین RNAseq و microarray» نسبت دادند.
چگونه میتوان این روش را در کلینیک بهکار برد؟
کاپور که مدیر یک مرکز پزشکی در پنسیلوانیا است نیز به این موضوع علاقهمند است. وی گفت:«در یک کلینیک، براشینگ بینی بهراحتی انجام میشود و برای جمعآوری به ابزارهای ماشینی نیاز ندارد. از آنجا که انجام براشینگ تنها چند ثانیه طول میکشد و تفسیر آن بهصورت خودکار انجام میشود، تشخیص دقیق آنی آسم برای ارائهدهندگان مراقبتهای اولیه بسیار مفید خواهد بود.
Dr.Augusto A.Litonjua متخصص آسم و استاد متخصص اطفال در مرکز پزشکی دانشگاه روچستر، بر این باور است که استفاده از زیستشناسی سیستمها برای ایجاد طبقهبندی آسم همانطور که Bunyavanich انجام داده است «امیدوارکننده و نویدبخش» است.
او میگوید:«این تست میتواند مشکلی که در حال حاضر در کلینیک به آن پرداخته نمیشود را حل کند. محققان آسم سالهاست که میدانند اشکال مختلفی از آسم وجود دارد؛ آسم یک بیماری نیست بلکه احتمالاً مخلوطی از چندین بیماری است که یک فنوتیپ نهایی مشترک دارند. ما تلاش کردهایم که با استفاده از مارکرهای فنوتایپیک یا بیومارکرهای خونی، آسم را به زیرفنوتیپهایی طبقهبندی کنیم. این کار ممکن است منجر به ایجاد راهی سادهتر در خصوص بهدست آوردن نمونههایی جهت طبقهبندی انواع مختلف آسم باشد. این روش چنانچه اعتباربخشی شود میتواند کاربرد گستردهای در مقیاس بالینی داشته باشد».
چه اعتباربخشیهای دیگری باید انجام شود؟
Litonjua گفت: اعتبار در جمعیتهای مختلف با استفاده از انواع مختلف آسم (آلرژیک در مقابل غیرآلرژیک) و در گروههای سنی مختلف (آسم کودکان در مقابل آسم بزرگسالان) است، بهعلاوه برای طبقهبندی، مطالعهها باید با استفاده از این روش انجام شود تا مشخص شود که آیا نشانهای وجود دارد که بتواند پاسخ به درمان را بهصورت دقیق پیشگویی کند.
Bunyavanich نیز موافق است که آنها باید اعتباربخشی را در گروههای بزرگتر انجام دهند و با مؤسسه او همکاری نموده تا چگونگی پیشرفت این تکنولوژی فوق را مشاهده نمایند.
او گفت:«من دیروز در کلینیک بودم، هرکسی که علائم بیماری را شرح میداد، ما برسهایی داشتیم و با برس و سواب از بینی نمونه میگرفتیم. این کار تنها به چند ثانیه زمان نیاز داشت. این الگوریتم بهصورت خودکار انجام میشود و میتواند در همان روز یا روز بعد پاسخ را برای مدیریت و درمان تحویل دهد».
فراپژوهش